Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào các loại A, loại B, loại C, loại D như thế nào?
- Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại A như thế nào?
- Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại B như thế nào?
- Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại C như thế nào?
- Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại D như thế nào?
Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại A như thế nào?
Theo Quy tắc 5 Phần III Phụ lục I ban hành kèm theo Thông tư 39/2016/TT-BYT quy định như sau:
"Quy tắc 5. Các trang thiết bị y tế chẩn đoán in vitro được phân vào loại A nếu thuộc một trong các trường hợp sau:
1. Là thuốc thử hoặc các sản phẩm khác có tính chất đặc thù được chủ sở hữu chỉ định dùng cho các quy trình chẩn đoán in vitro liên quan đến xét nghiệm cụ thể.
2. Là trang thiết bị được chủ sở hữu chỉ định sử dụng trong các quy trình chẩn đoán in vitro.
3. Vật chứa mẫu."
Theo đó nếu thuộc các trường hợp trên thì trang thiết bị y tế chẩn đoán in vitro sẽ được phân vào loại A.
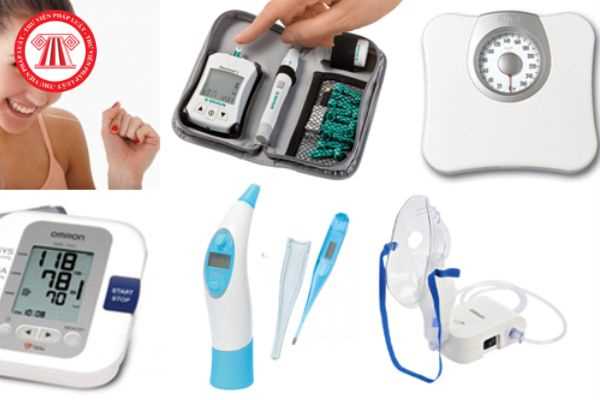
Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào các loại A, loại B, loại C, loại D như thế nào? (Hình từ Internet)
Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại B như thế nào?
Căn cứ Quy tắc 6 và Quy tắc 7 Phần III Phụ lục I ban hành kèm theo Thông tư 39/2016/TT-BYT thì các loại trang thiết bị y tế chẩn đoán in vitro sẽ được phân vào loại B nếu không thuộc loại A, C và D.
Tuy nhiên đối với các trang thiết bị y tế chẩn đoán in vitro là các vật liệu kiểm soát thì không được gán giá trị định lượng hoặc định tính thuộc loại B.
Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại C như thế nào?
Căn cứ theo Quy tắc 3 Phần III Phụ lục I ban hành kèm theo Thông tư 39/2016/TT-BYT thì các trang thiết bị y tế chẩn đoán in vitro được phân vào loại C khi thuộc các trường hợp:
"Quy tắc 3. Trang thiết bị y tế chẩn đoán in vitro sử dụng cho một trong các mục đích sau thì được xếp vào loại C
1. Phát hiện sự hiện diện hoặc phơi nhiễm với tác nhân lây truyền qua đường tình dục (ví dụ những bệnh lây truyền qua đường tình dục, Chlamydia trachomatis, Neisseria gonorrhoeae).
2. Phát hiện sự hiện diện của tác nhân truyền nhiễm trong dịch não tủy hoặc máu với khả năng lây truyền hạn chế (ví dụ Neisseria meningitidis hoặc Cryptococcus neoformans).
3. Phát hiện sự hiện diện của tác nhân truyền nhiễm mà khi kết quả xét nghiệm sai có nguy cơ rất lớn dẫn đến tử vong hoặc khuyết tật nghiêm trọng cho cá nhân hoặc thai nhi được xét nghiệm (ví dụ xét nghiệm chẩn đoán CMV, Chlamydia pneumoniae, Staphylococcus aureus kháng Methycillin).
4. Sàng lọc trước sinh để xác định tình trạng miễn dịch đối với các tác nhân gây bệnh truyền nhiễm (ví dụ kiểm tra tình trạng miễn dịch đối với Rubella hoặc Toxoplasmosis).
5. Xác định tình trạng bệnh truyền nhiễm hoặc tình trạng miễn dịch mà kết quả xét nghiệm sai có thể dẫn đến nguy cơ đe dọa tính mạng bệnh nhân trong thời gian gần do quyết định điều trị không phù hợp (ví dụ xét nghiệm chẩn đoán Enterovirus, CMV và HSV ở bệnh nhân được cấy ghép).
6. Sàng lọc lựa chọn bệnh nhân để áp dụng biện pháp quản lý và liệu pháp điều trị phù hợp hoặc để xác định giai đoạn của bệnh hoặc chẩn đoán ung thư (ví dụ y học cá thể hóa).
Các trang thiết bị y tế chẩn đoán in vitro mà quyết định điều trị thường chỉ được đưa ra sau khi có đánh giá sâu hơn và những thiết bị y tế chẩn đoán in vitro được sử dụng để theo dõi sẽ thuộc loại B theo quy tắc 6 - Phần III.
7. Xét nghiệm gen di truyền ở người (ví dụ như bệnh Huntington, xơ nang).
8. Theo dõi nồng độ thuốc, các chất hoặc các thành phần sinh học mà kết quả xét nghiệm sai có thể dẫn đến nguy cơ đe dọa tính mạng bệnh nhân ngay tức thì do quyết định điều trị không phù hợp (ví dụ như các dấu hiệu tim mạch, cyclosporin, xét nghiệm thời gian đông máu).
9. Theo dõi, điều trị bệnh nhân bị bệnh truyền nhiễm đe dọa tính mạng (ví dụ như tải lượng virus HCV, tải lượng virus HIV và xác định kiểu gen, phân nhóm kiểu gen HIV, HCV).
10. Sàng lọc rối loạn bẩm sinh ở thai nhi (ví dụ như tật nứt đốt sống hoặc hội chứng Down)."
Đồng thời tại Quy tắc 4 Phần này còn quy định:
- Trang thiết bị y tế chẩn đoán in vitro tự xét nghiệm sẽ được phân vào loại C.
Trường hợp kết quả xét nghiệm của trang thiết bị y tế chẩn đoán in vitro không phục vụ quyết định điều trị hoặc chỉ có giá trị tham khảo và cần thực hiện xét nghiệm bổ sung phù hợp tại phòng xét nghiệm thì trang thiết bị này thuộc loại B.
- Các trang thiết bị y tế chẩn đoán in vitro dùng để xét nghiệm tại chỗ thông số khí máu và đường huyết cũng thuộc loại C.
Các trang thiết bị y tế chẩn đoán in vitro xét nghiệm tại chỗ khác được phân loại dựa trên các quy tắc phân loại tương ứng.
Quy tắc phân loại trang thiết bị y tế chẩn đoán in vitro vào loại D như thế nào?
Căn cứ Quy tắc 1 và Quy tắc 2 Phần III Phụ lục I ban hành kèm theo Thông tư 39/2016/TT-BYT thì các trang thiết bị y tế chẩn đoán in vitro sau sẽ được phân vào loại D:
- Sử dụng để phát hiện sự hiện diện hoặc sự phơi nhiễm với một tác nhân lây nhiễm trong máu, thành phần máu, dẫn xuất máu, tế bào, mô hoặc các bộ phận cơ thể người nhằm đánh giá sự phù hợp của chúng để thực hiện truyền máu hoặc cấy ghép.
- Sử dụng để phát hiện sự hiện diện hoặc sự phơi nhiễm với một tác nhân lây nhiễm mà tác nhân đó gây ra bệnh đe dọa đến tính mạng, thường không có khả năng chữa trị với nguy cơ lây truyền cao.
- Trang thiết bị y tế chẩn đoán in vitro được sử dụng để xác định nhóm máu hoặc phân loại mô để bảo đảm tương thích miễn dịch của máu, thành phần máu, các tế bào, mô hoặc bộ phận cơ thể để thực hiện truyền máu hoặc cấy ghép thì được xếp vào loại C, trừ trang thiết bị y tế sử dụng để xác định nhóm máu hệ ABO [A (ABO1), B (ABO2), AB (ABO3)], hệ rhesus [RH1 (D), Rh2 (C), Rh3 (E), RH4 (c), RH5(e)], hệ Kell [Kel1 (K)], hệ Kidd [JK1 (Jka), JK2 (Jkb)] và hệ Duffy [FY1 (Fya), FY2 (Fyb)].









Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.
- Thay đổi hương liệu làm thay đổi thành phần cấu tạo của sản phẩm thì có phải công bố lại sản phẩm không?
- Hội đồng kiểm định chất lượng giáo dục do ai thành lập? Thành lập hội đồng kiểm định chất lượng giáo dục nhằm mục đích gì?
- Cắt tải sự cố là gì? Đơn vị phát điện có trách nhiệm thực hiện cắt tải sự cố theo yêu cầu của ai?
- Kỷ niệm chương của Ủy ban Thường vụ Quốc hội có tên gọi là gì? Tiêu chuẩn xét tặng Kỷ niệm chương quy định ra sao?
- Công văn 5423/SYT-NVY kích hoạt ứng phó Covid 19 trước biến thể Omicron XEC tại Thành phố Hồ Chí Minh?








